Тонус в руке после инсульта. Спастичность после инсульта: как действовать, чтобы жить? судороги после инсульта
В зависимости от области мозга, пораженной в результате инсульта, могут поменяться некоторые телодвижения, речь и функции организма. Отдельные области мозга наделены своими собственными функциями и контролируют конкретные части тела. Прогноз для больного инсультом зависит от места поражения болезнью и тяжести повреждения мозга. Это, как известно, не редкость для рук, которые становятся слабыми после инсульта. Использование препаратов и правильно подобранных упражнений для укрепления мышц могут вернуть контроль и силу в мышцы рук, что вернет вас к состоянию нормального человека.
Шаги
Часть 1
возврат сил при помощи упражнений- Сгибание плеча. Держа в руках гантель, поддерживайте прямой локоть и поднимите руку над головой и опустите ее вниз. Повторите это упражнение десять раз. Возьмите гантель в другую руку и повторите то же самое упражнение. Выполняйте его, по крайней мере, один раз в день.
- Отведение плеча. Удерживайте гантель в одной руке, держа ее прямо. Затем отведите руку в сторону на высоте плеч. Верните руку к себе. Повторите это десять раз, а затем переключитесь на другую руку. Повторяйте это упражнение также не менее одного раза в день.
-
Также разрабатывайте локти. Вот два упражнения, которые вы можете выполнять для укрепления своих локтей, предплечья и кистей рук:
- Разведение локтей. Наклонитесь немного вперед и задержите локти позади себя. Поднимите гантель сзади вас, поддерживая локти прямыми, а затем согните их. Повторите так десять раз, а затем поменяйте руки и повторите это с другой стороны.
- Сгибание локтей. Возьмите гантель одной рукой. Затем, согните руку в локте, а после выпрямите ее. Повторите это десять раз. Поменяйте сторону и повторите, либо выполняйте упражнение на оба локтя одновременно.
-
Также делайте повороты. Для укрепления рук, кистей и пальцев и укрепления мышц, вы можете делать повороты в дополнение к сгибательным и разгибательным упражнениям. Вот два типа поворотных упражнений, которые помогут укрепить ваши мышцы:
- Внешние развороты . Возьмите в руки эластичный резиновый жгут. Начните упражнение с согнутых в 90 градусов к телу локтей. Поверните руки, повернув ладони в стороны. Повторите это десять раз. Выполняйте его, по крайней мере, один раз в день.
- Внутренние вращения. Привяжите один конец резинки к дверной ручке. Затем, поддерживая локоть под углом 90 градусов, потяните другой ее конец в направлении живота. Выполняйте это упражнение также не менее одного раза в день.
-
Укрепите свои запястья. Упражнения на запястья за счет использования гантели считаются несущими весовую нагрузку упражнениями. Такой вид физической активности приводит к образованию новой костной ткани, и он делает кости сильнее. Вместе с увеличением кровотока при физической нагрузке также увеличивается мышечная масса и сила. Может быть выполнено следующее:
- Возьмите в обе руки по гантеле при локтях, согнутых на 90 градусов. Поверните ладони вверх и вниз десять раз. Выполняйте это упражнение, по крайней мере, один раз в день.
- С ладонями вниз держите в каждой руке по гантеле и сгибайте локти до 90 градусов. Поднимите запястья вверх и вниз, сохраняя при этом локти в исходном положении. Повторите это десять раз. Как обычно, выполняйте это, по крайней мере, один раз в день.
-
Поймите суть действия этих упражнений. Такие упражнения, как сгибание и отведение плеча, сгибание и разгибание локтей, внешние и внутренние вращения разрабатывают мышцы рук, локтей, запястий и плеч. Разработка поврежденной части тела через потягивания, толчки или подъемы стимулирует рост мышц и увеличивает их эффективность. Регулярные физические упражнения увеличивают в каждой клетке количество миофибрилл (мышечных волокон), что составляет от 20 до 30% роста мышечной массы.
- Из-за увеличения кровотока в мышечные волокна подается больше кислорода и питательных веществ, ведущих к увеличению мышечной массы. Увеличение мышечной массы приводит к увеличению и мышечной силы. Когда мышцы начинают работать, они развивают больше митохондрий, маленьких электростанций, которые преобразовывают химическую энергию в энергию, используемую клетками.
Часть 2
использование медикаментозного подхода-
Принимайте от 40 до 80 мг баклофена (лиоресаля) каждый день. Этот препарат действует на центральную нервную систему, предотвращая нервные импульсы в головном мозге, которые заставляют сокращаться мышцы. Он расслабляет мышцы, уменьшая мышечные спазмы, стеснение, боль, и увеличивает диапазон движений. Для взрослых необходимая доза баклофена составляет 40-80 мг/сутки для четырех отдельных доз.
- Аналогом лекарства баклофен является дантролен натрия (дантриум). Рекомендуемая доза составляет от 25 мг до максимальной 100 мг три раза в день.
-
Попробуйте 8 мг тизанидина гидрохлорида (занафлекс) каждые 6 или 8 часов. Этот препарат также блокирует нервные импульсы в мозге, которые заставляют сокращаться мышцы. Идеально подходящая начальная доза составляет 4 мг каждые 6 или 8 часов. Поддерживающая доза составляет 8 мг каждые 6 или 8 часов.
- Тем не менее, эффективность препарата длится только в течение короткого периода времени, так что желательно использовать его по необходимости для облегчения дискомфорта и возможности выполнять определенные действия.
-
Рассмотрите возможность принятия бензодиазепинов, таких, как валиум и клонопин. Этот тип лекарства действует на центральную нервную систему, тем самым расслабляя мышцы и снижая спастику в течение короткого промежутка времени.
- Пероральная доза изменяется, поскольку бензодиазепины выходят под разными названиями (другими словами, существуют различные медицинские названия этого препарата). Проконсультируйтесь со своим врачом для подбора подходящего состава.
-
Рассмотрите получение инъекций ботулинического токсина (ботокса), чтобы уменьшить спастику. Инъекции ботокса прикрепляются к нервным окончаниям и блокируют высвобождение химических переносчиков, которые сигнализируют мозгу активировать мышечное сокращение. По сути, лечение предотвращает мышечные спазмы.
-
В качестве альтернативы рассмотрите инъекции фенола. Фенол разрушает нервную проводимость, которая вызывает спастику. Он используется в виде инъекций непосредственно в пораженные мышцы или в позвоночник. Дозировка может варьироваться в зависимости от производителя.
- Проконсультируйтесь со своим врачом о том, подходит ли вам этот курс лечения. Инъекции фенола подходят не всем пациентам, перенесшим инсульт.
-
Поговорите со своим врачом о терапии с электрической стимуляцией. Эта терапия позволяет стимулировать пораженные нервные окончания в мозге, чтобы заставить сокращаться мышцы. Такая терапия помогает восстановить движение и контроль рук и кистей, улучшает мышечный тонус и уменьшает болевые ощущения пациента после инсульта. Она также увеличивает приток крови к мозгу, чтобы ускорить заживление и уменьшить отек, улучшает приток лекарств к коже и уменьшает мышечную спастику.
- Опять-таки, электрическая терапия подходит не всем. Только ваш лечащий врач знает, подходит ли вам эта процедура.
-
Проконсультируйтесь с физиотерапевтом для начала мышечной терапии. Есть два типа восстановления мышц, которые вы, возможно, захотите рассмотреть:
- Ограниченно-индуцированная двигательная терапия. Эта терапия часто выполняется в период реабилитации, чтобы увеличить способность мозга к самовосстановлению и пострадавшие руки к восстановлению своих функций. Движения здоровой рукой сдерживаются с помощью устройства, чтобы позволить использовать поврежденную руку для как можно большей деятельности.
- Реабилитационная терапия. Реабилитационная терапия (РТ) помогает пациенту после инсульта заново научиться его повседневным занятия, привычным до болезни. Это позволит ускорить восстановление, так как вы будете учиться жить и работать с ограниченными возможностями. Врач поможет вам переоборудовать ваше жилице для более безопасного и легкого передвижения внутри него.
-
Поработайте с командой по реабилитации после инсульта, чтобы определить, какое лечение подходит вам лучше всего. Возврат силы в руки не означает, что вы пользуетесь исключительно одним лекарством или видом лечения. Во время реабилитации после инсульта вы и реабилитационная команда будете работать вместе, чтобы определить, какие лекарства работают хорошо, и что улучшает ригидность после инсульта в ваших руках.
- Лекарства не являются панацеей от инсульта: они только облегчают симптомы спастики, которые сковывают мышцы. Спастика мышц причиняет боль, нарушает положение тела и приводит к неконтролируемым движениям. Руки могут начать восстанавливать свою нормальную силу и широту движений, если лекарства, принимаемые больным, облегчают спастику.
Часть 3
понимание своего состояния-
Будьте в курсе перенесенного типа инсульта. Когда приток крови к области мозга затруднен, он приводит к развитию инсульта. Клетки мозга, которые не снабжаются кровью, умирают из-за недостатка кислорода. В считанные минуты и без предупреждения инсульт может произойти и поразить человека. Различают два типа инсульта:
- Ишемический инсульт. Это наиболее распространенный вид инсульта. Около 87% пациентов, перенесших инсульт, страдают от этого типа. Он развивается из-за тромба в кровеносном сосуде, который вызывает прерывание потока крови к мозгу. Он также может быть вызван эмболиями или тромбом, который перемещается в другие части тела.
- Геморрагический инсульт. Разрыв кровеносных сосудов на поверхности мозга, которые заполняют пространство между черепом и мозгом, приводит к геморрагическому инсульту. Геморрагический инсульт может также быть вызван разрывом артерии в мозге, который вызывает кровотечение в соседние ткани.
-
Узнайте, какие симптомы могут быть вызваны инсультом. Пациенты, перенесшие инсульт, могут испытывать слабость с одной стороны тела, могут быть затронуты либо руки, либо ноги, или обе части тела. Могут быть также и речевые нарушения, проблемы со зрением, памятью и умом, трудности при глотании, недержание мочи и проблемы с мочевым пузырем. При серьезном случае инсульта может случиться паралич или даже смерть.
- Руки и ладони после инсульта могут стать особенно чувствительными. У больного с инсультом может случиться приступ спастики, неконтролируемое сжимание и скованность мышц, что вызывает трудности в движении рукой с ладонью. Поврежденная рука или нога находятся на противоположной стороне тела от пораженной инсультом части головного мозга.
Разрабатывайте свои плечи. По данным Американской кардиологической ассоциации повторное использование пораженных частей тела, таких, как руки, ладони и пальцы выявляют новые способы взаимодействия между мозгом и пораженной областью. Движения и физиотерапия помогают пациентам после инсульта переучивать мозг использовать навыки мелкой моторики. Упражнения для развития плеч следующие:
Снять спастику после инсульта оказалось чрезвычайно трудно. Дело в возникающем противоречии. Мы упёрто восстанавливали силу и выносливость. Делали это с помощью специальных упражнений с высокой нагрузкой и кучей повторений.
Для лечения спастики это помеха и вред. При снятии спастики нужен расслабляющий массаж и легкие движения в упражнениях. Что бы продолжить восстановление после инсульта надо проводить взаимоисключающие занятия. Но мы придумали простое решение. Сделать две группы занятий.
Первая: для восстановления силы и выносливости. Вторая для лечения спастики, восстановления равновесия и координации. Решение оказалось очень правильным. Правда мы допёрли до него не сразу и некоторое время делали упражнения для снятия спастики вместе с упражнениями на силу и выносливость. Вовремя заметили, что от активных упражнений спастика усиливается.
Что из себя представляет спастика
Проявляется спастика в скованности. Невозможно сделать быстрое или резкое движение. Постоянно напряженные мышцы блокируют свободу
. Чувство словно ты сильно заржавевший Терминатор))).
Напряжение приводит к скорой утомляемости.
Восстановление после инсульта может быть фактически заблокировано спастикой. Трудно восстанавливать навыки, когда конечности словно связаны резинками и всегда находятся в напряженном, неестественном положении. Для снятия спастики после инсульта мы применяем элементарные упражнения. Главное делать их легко, без напряжения.
Спастика мышц — это непроизвольное их сокращение, судороги или спазм вследствие нарушения проводимости нервных импульсов после травмы спинного и головного мозга.
Чаще это состояние проявляется ночью, но так же может существенно затруднить жизнь днем.
Механизм образования спастичности
Основной причиной формирования судорог специалисты называют дисбаланс тормозного влияния двигательных элементов коры головного на клетки в структуре спинного мозга.
Закономерным итогом становится растормаживание тонического рефлекса – формируется мышечная спастика в пораженных травмой конечностях человека.
В нормальном состоянии человеку не приходиться задумываться об очередности производимых в мышцах явлениях: какие из них сначала требуется сократить, затем расслабить – наш мозг довел подобную деятельность до автоматизма.
После инсульта или травмы происходит гибель клеточных элементов, несущих ответственность за специальные тормозящие импульсы в двигательных нейронах головного и спинного мозга. Рефлекторная дуга: конечность – спинной мозг – головной мозг перестает быть единой системой – происходит нарушение координации.
Спазмы формируются далеко не сразу – на протяжении недель , и даже месяцев. Приводит к значительным вторичным изменениям в мышцах и суставах – усиливает отрицательное воздействие парезов на двигательную систему.
Степень выраженности спастики конечностей
Первые признаки начала формирования спастики мышц наблюдаются в первые же сутки после травмы, а в последующем имеют тенденцию к усилению.
Изменяться степень выраженности может под неблагоприятным воздействием негативных факторов, к примеру:
- при изменении эмоциональной настроенности – наличии у человека склонности к депрессивным состояниям;
- при изменении погодных условий – колебание параметров температуры либо освещенности;
- при чрезмерной физической перегрузке, вызванной ранней физической активностью пострадавшего, вопреки рекомендациям врача.
При усилении интенсивности нагрузки на мышечные волокна в конечностях, происходит затруднение их двигательной активности, наблюдаются симптомы болевых ощущений в них, различной степени выраженности.
По степени выраженности спастики различают следующие формы:
Спастика ног в легкой форме проявляется быстрой утомляемостью мышц голеней, ощущение «забитости мышц», от физической деятельности, ходить при этом легче становится на каблуке, затем становится затруднительно потянуть к себе пальцы ног и разогнуть ее в колене.
В тяжелой форме спазма: одна или две ноги фиксируются в согнутом в коленном или тазобедренном суставах, а стопа выворачивается внутрь или наружу. При хождении без специальной обуви или , могут возникнуть деформации или контрактуры.
Проявление спастике рук в легкой форме: затруднено разгибание
пальцев и выпрямление руки в локтевом суставе, признаком тяжелой формы является согнутые в локтевом и плечевом суставах, кисть при этом сжата в кулак.
Если спастика присутствует долгое время без лечения, развивается контрактура, то есть сустав фиксируется не в физиологическом для организма состоянии.
В дальнейшем же, спазм будет иметь лишь отрицательное влияние на проведение восстановительных мероприятий. Помимо конечностей, будет ухудшать восстановление и в позвоночнике: повышение тонуса мышц вызывает болевые ощущения в спине – симптомы вертеброгенного радикулита.
Специалисты отмечают: чем раньше было начато адекватное лечение современными препаратами, а также, чем меньше выраженность спастики– тем лучше будет прогноз реабилитационных мероприятий.
Даже, если симптомы значительно выражены, а лечение судорог в силу определенных причин начались в более поздний временной промежуток – уменьшение спастики существенно улучшает общее самочувствие.
Как нужно лечить спастику разными методами
Наиболее важным требованием, предъявляемым к лечению, является его максимально возможная безболезненность, поскольку боль многократно усиливается спастикой.
Важным моментом является и контроль за деятельностью тазовых органов – предупреждение воспалительных проявлений в них, а также своевременно проводить мероприятия по предупреждению возникновения контрактур и .
 Комплекс современного лечения по избавлению от спастики:
Комплекс современного лечения по избавлению от спастики:
- лекарственная тактика (мидокалм, баклофен);
- методики;
- ортезирование;
- хирургическая коррекция.
Комплекс лечения подбирается только индивидуально, в прямой зависимости от локализации очага и степени выраженности спастики. Необходимо учитывать и технические возможности медицинского учреждения.
Спастика после инсульта или травмы головного мозга обязательно требует медикаментозного воздействия. Лечение должно проводиться поэтапно – с постепенным наращиванием лечебной дозы медикаментов, возможно заменой препарата.
 На сегодняшний день востребованы две подгруппы:
На сегодняшний день востребованы две подгруппы:
- Препараты с центральным механизмом воздействия на негативный очаг – торможение рефлекса.
- Препараты периферического воздействия – существенно снижают рефлекс растяжения на уровне элементов спинного мозга: миорелаксанты.
Как и у иных подгрупп даже самых современных препаратов, у вышеперечисленных имеют свои противопоказания, поэтому их назначением должен заниматься только высококвалифицированный специалист невролог.
Ортезирование и гипс
Лечение спастики длительной укладкой конечностей человека, в такое положение, когда мышцы оптимально растянуты, а тоническая рефлекторная активность уменьшена, именуется специалистами ортезированием. Оно способствует снижению гипертонуса в конечностях – патологические симптомы удается многократно уменьшить.
При выраженной спастике рекомендуется даже наложение специальной гипсовой лангеты либо шины – для предотвращения развития контрактуры. Именно шина фиксирует конечность в наиболее приемлемом положении — при котором мышечные волокна располагаются в растянутом положении.
Лечение ортезированием проводится от одного до двух часов, в прямой зависимости от ощущений человека – при усилении болевых ощущений, процедуру заканчивают.
Физиотерапия при скованности мышц
- локальное использование холода – способствует понижению чрезмерных рефлексов и максимальному увеличению объема движений, улучшению деятельности мышц;
- локальное использование тепла – отлично способствует временному понижению тонуса. осуществляется при помощи озокеритовых или парафиновых аппликаций, курс – не менее двадцати процедур;
- нервных окончаний – превосходная методика, позволяющая добиться максимального ответа в пораженных участках, продолжительность лечебного курса назначается специалистом.
ЛФК разработка
 Лечение с помощью упражнений, направленных на оптимальное расслабление волокон в мышцах – давно проверенный, успевший себя отлично зарекомендовать реабилитационный прием лечения спастики.
Лечение с помощью упражнений, направленных на оптимальное расслабление волокон в мышцах – давно проверенный, успевший себя отлично зарекомендовать реабилитационный прием лечения спастики.
Дозированное лечебное растягивание позволяет на пару часов понизить их тонус, максимально увеличить объем движений в пораженных конечностях.
Кинезиотерапевт знает, что снижение тонуса будет наблюдаться лишь определенное время а потому его необходимо эффективно использовать для проведения иных комплексных упражнений, которые были затруднены из-за спастики.
Хирургическое вмешательство определяется специалистом по строго индивидуальным показаниям, когда консервативные методики уже исчерпали себя, а выраженной положительной динамики не наблюдается.
Снять спастику задача важная. Она сильно мешает в повседневной жизни, отнимает силы и сковывает движения. Это мешает восстанавливать утраченные навыки и выносливость. Чтобы полноценно проводить восстановление после инсульта, нужно обязательно вылечить спастику. Мы это выполняем параллельно с остальными задачами.
При комплексном подходе и начале лечебных мероприятий на возможно более раннем этапе, медикаментозного лечения – нормализация мышечного тонуса способствует максимальному ускорению восстановления больного.
В лечении хорошо себя показали такие методы как, миостимуляция,ботокс, конечно лечебная гимнастика, медицинские препараты(мидокалм, баклофен) и щадящая хирургия.
Что такое, причины возникновения спастичности, недопущение и лечение обновлено: Ноябрь 21, 2017 автором: автор
Для цитирования:
Дамулин И.В. Спастичность после инсульта // РМЖ. 2005. №7. С. 501
Инсульт остается крайне важной медико–социальной проблемой, поскольку является одной из наиболее частых причин инвалидизации, в большинстве случаев связанной с двигательными нарушениями . У 80–90% больных в остром периоде инсульта выявляется гемипарез, остаточные явления перенесенного инсульта различной степени выраженности и характера отмечаются примерно у 2/3 больных. Почти 3/4 лиц с инсультом – в возрасте 65 лет и старше, при этом частота инсульта примерно на 20% выше у мужчин, чем у женщин.
Более чем у 50% пациентов имеется артериальная гипертензия, у 25% – сахарный диабет, почти у 25% – указание в анамнезе на перенесенный в прошлом инсульт. Помимо артериальной гипертензии и сахарного диабета, факторами риска развития инсульта являются поражения магистральных сосудов головного мозга, фибрилляция предсердий, курение, гиперлипидемия и повышенный уровень фибриногена. У лиц молодого возраста среди основных факторов риска развития инсульта следует отметить церебральные эмболии, травму экстракраниальных сосудов, васкулопатии различного генеза, нарушения коагулогических свойств крови, использование оральных контрацептивных препаратов, роды, наркоманию (особенно кокаиновую зависимость), а также заболевания, связанные с ВИЧ–инфицированием. Следует заметить, что кокаин приводит к цереброваскулярным нарушениям, воздействуя на артериальное давление и тонус сосудов, вызывая длительный вазоспазм, увеличивая синтез тромбоксана и повышая склонность тромбоцитов к тромбообразованию, при этом также увеличивается риск возникновения кардиогенных эмболий . Хроническое употребление кокаина приводит к церебральной атрофии и патологии белого вещества полушарий головного мозга . По данным методов функциональной нейровизуализации выявляются множественные зоны церебральной гипоперфузии . Довольно характерны для этой категории больных нарушения лобного типа, проявляющиеся, в частности, увеличением числа ошибок персеверативного типа при выполнении Висконсинского теста сортировки карточек . Васкулиты являются причиной лишь 3–5% инсультов у лиц моложе 50 лет . Заболеваемость церебральными васкулитами составляет 1–2 случая на 1 млн населения в год (для сравнения: системными васкулитами – 39 случаев) . Основным механизмом, приводящим к поражению нервной системы при васкулитах, является ишемия . Возникновение ишемии при воспалении стенки сосудов связано с тремя патогенетическими факторами: обструкцией сосудов, увеличением склонности к коагуляции крови, что обусловлено влиянием провоспалительных цитокинов на поверхность эндотелия и изменением сосудистого тонуса . Однако чаще при васкулитах поражаются сосуды висцеральных органов или сосуды, кровоснабжающие периферические нервы . Возможно, это обусловлено особенностями строения стенки церебральных сосудов (в частности, лимфоцитарная адгезия эндотелия церебральных сосудов меньше 5%, в других органах – 15–20%) и наличием гематоэнцефалического барьера .
Одним из серьезных осложнений перенесенного инсульта является спастичность в пораженных конечностях, которая отмечается почти у 65% больных, перенесших инсульт. У больных со спастичностью существенно возрастает риск падений и, соответственно, травматизации, нередко возникают контрактуры, болевые синдромы, пролежни, остеопороз, тазовые расстройства и тромбофлебиты. Непосредственной причиной летального исхода этой категории больных могут быть сердечно–сосудистые, легочные или почечные осложнения.
Под спастичностью понимается двигательное расстройство, которое характеризуется скорость–зависимым повышением тонических рефлексов растяжения в результате поражения верхнего мотонейрона . Клинически это проявляется повышенным мышечным сопротивлением, варьирующим по своей выраженности в зависимости от амплитуды и угловой скорости производимого пассивного движения. Характерным для спастичности признаком является феномен «складного ножа», когда при пассивном сгибании пораженной конечности выраженное в начале движения сопротивление мышцы внезапно сменяется ее сокращением в направлении производимого движения. Спастичность, как правило, сопровождается парезом и иной симптоматикой, характерной для поражения верхнего мотонейрона. Среди клинических признаков поражения верхнего мотонейрона выделяют т.н. «позитивные» и «негативные» симптомы, а также изменения спастически сокращенных мышц (табл. 1).
Сразу после развития инсульта мышечный тонус в паретичных конечностях чаще снижен, однако в течение 2–3 дней он повышается, приводя, в конечном счете, к характерной позе с повышением тонуса в аддукторах и флексорах руки и аддукторах и экстензорах ноги. Легкие изменения в двигательной сфере в виде некоторого снижения мышечной силы и оживления рефлексов могут отмечаться и на ипсилатеральной стороне. Повышение мышечного тонуса в паретичных конечностях может возникать не только по прошествии нескольких дней от начала заболевания, но и спустя более продолжительный период времени (через недели и даже месяцы) .
Выраженность клинических проявлений может варьировать в зависимости от локализации очага, объема пораженной ткани и длительности заболевания. Регуляция мышечного тонуса осуществляется под влиянием как центральной, так и периферической импульсации на a–мотонейроны спинного мозга. a–мотонейроны, которые иннервируют мышечные волокна, располагаются в области передних рогов спинного мозга. Афферентные импульсы от рецепторов в мышцах передаются к структурам спинного мозга по сенсорным волокнам. Сенсорные волокна заканчиваются на a–мотонейронах передних рогов (моносинаптические пути), а также на вставочных нейронах задних рогов спинного мозга, связанных, в свою очередь, с двигательными нейронами, иннервирующими мышцы–антагонисты (полисинаптические пути). В основе возникновения спастичности лежит нарушение тормозящих влияний супраспинальных отделов на спинальные двигательные и вставочные нейроны. При этом на спинальном уровне возникает нарушение баланса между процессами возбуждения и торможения, а также денервационная гиперчувствительность и нейрональный спраутинг. Высказывавшееся ранее предположение о селективной гиперактивности g–системы, как одном из ведущих патогенетических механизмов спастичности, достоверных экспериментальных подтверждений не нашло.
При длительно существующем пирамидном синдроме определенное влияние на повышение мышечного тонуса оказывают также изменения самих мышц (табл. 2).
Ряд из этих расстройств (изменение реакции на растяжение, нарушение быстрого расслабления мышечного волокна, нарушение реципрокного ингибирования, нарушение сократительных способностей мышцы вследствие изменения структуры мышечного волокна, вторичное возникновение боли и нарушение способности мышц–антагонистов оказывать сопротивление, сопоставимое с действием спастически измененных мышц) могут быть уменьшены при использовании методов хемоденервации мышц или введении препаратов ботулинического токсина. Однако снижение мышечной силы и увеличение латентного периода активации мышцы при подобном лечении могут нарастать .
Несмотря на то, что спастичность считается одним из характерных признаков поражения кортикоспинального пути, в основе ее возникновения лежит поражение экстрапирамидных двигательных путей. Важную роль в регуляции мышечного тонуса играют ретикулоспинальные и вестибулоспинальные нисходящие пути. Само по себе изолированное поражение пирамидных путей на уровне коры, ножек мозга, основания моста или пирамид продолговатого мозга не сопровождается повышением мышечного тонуса .
В реабилитационном периоде после инсульта вначале происходит восстановление движений в проксимальных отделах конечностей, затем – в дистальных. Обычно при инсульте соответствующей локализации слабость в верхних конечностях возникает раньше, чем слабость в нижних конечностях, и, как правило, восстановление нормальных двигательных функций в гемипаретичной руке происходит хуже, чем в ноге. Одним из объяснений этому является то, что функциональное восстановление в руке включает не только регресс мышечной слабости, но также восстановление способности к выполнению тонких скоординированных движений. В отличие от этого функциональное восстановление в ноге, что проявляется восстановлением ходьбы, может протекать даже при незначительном или умеренном нарастании мышечной силы. Кроме того, успех реабилитационных мероприятий в руке может быть в значительной мере ограничен из–за присоединения изменений в плечевом суставе и связанном с этим возникновением боли.
Существенно хуже прогноз восстановления двигательных функций в руке, если плегия отмечается сразу в начале заболевания, а также в случае, если через 4 недели от начала заболевания не происходит восстановления хватания рукой. Однако примерно у 9% больных с выраженным парезом в руке в остром периоде заболевания в последующем можно добиться удовлетворительного восстановления, а у 70% пациентов, у которых отмечается некоторое улучшение двигательных функций в течение первых 4 недель от начала заболевания, в последующем отмечается полное или значительное восстановление двигательных функций в руке. Считается, что если у пациента в течение первых 2 недель от начала инсульта отсутствуют активные движения в конечностях, то в дальнейшем полного регресса двигательных расстройств не будет . В случае самостоятельного полного восстановления утраченных двигательных функций длительность периода восстановления, как правило, не превышает 3 месяцев (обычно 1,5–2 месяца после инсульта), однако в ряде случаев некоторое улучшение может продолжаться до 6–12 месяцев и даже более длительный период времени.
Спастичность приводит к существенным функциональным расстройствам и нарушению качества жизни больных. Однако сама по себе спастичность не всегда требует лечения, а уменьшение повышенного мышечного тонуса не во всех случаях имеет позитивное значение для больного . Например, у ряда пациентов с выраженными парезами наличие спастичности в мышцах, анатомически и функционально препятствующих силе тяжести («антигравитационные» мышцы), может облегчать стояние и ходьбу. Кроме того, наличие повышенного мышечного тонуса может препятствовать развитию мышечных атрофий, отека мягких тканей и остеопороза, а также уменьшать риск развития тромбоза глубоких вен нижних конечностей. Показаниями для лечения спастичности являются лишь те случаи, когда вследствие повышенного тонуса мышц нарушается «функционирование, позиционирование или комфорт».
Основными задачами лечения являются не только уменьшение выраженности патологически повышенного тонуса мышц, но также снижение выраженности болевого синдрома, предотвращение развития контрактур, улучшение способности больного к самообслуживанию, облегчение проведения реабилитационных мероприятий. Поэтому, осматривая пациента со спастичностью, врач должен решить следующие задачи :
1. Выявить пациентов, являющихся кандидатами для проведения того или иного специфического метода антиспастической терапии.
2. Определить конкретный метод терапии, применение которого в плане восстановления двигательных функций может быть наиболее эффективным у данного больного (миорелаксанты, инъекции ботулинического токсина, местное введение фенола или алкоголя, дорсальная ризотомия).
3. Провести мониторинг динамики основных двигательных характеристик (мышечная сила, подвижность в суставах и т.д.) и функциональной активности больного (ходьба, способность к самообслуживанию, активность в обыденной жизни) на фоне терапии.
Таким образом, клиническая оценка спастичности должна проводиться не только с целью выявления пораженных мышц (или мышечных групп), но также для определения влияния существующей спастичности на все аспекты жизнедеятельности больного, включая способность к передвижению, трудоспособность и активность в повседневной жизни, что важно для планирования терапевтических программ (табл. 3). Для более детальной оценки может использоваться электромиография, а также диагностические локальные блокады с анестетиком, что помогает в выборе последующего метода лечения.
Оценивая повышение мышечного тонуса, следует учитывать и то, что он может существенно меняться в зависимости от позы больного и его эмоционального состояния . Усиление выраженности спастичности может происходить под влиянием внутренних факторов (при задержке мочеиспускания, воспалительных урологических заболеваниях, мочекаменной болезни, запорах) и внешних причин (переломы, неправильное положение спастической конечности в постели, тромбоз глубоких вен нижних конечностей).
Следует особо подчеркнуть, что спастичность клинически реализуется в различной форме и с участием разных механизмов, включая изменения как пресинаптического, так и постсинаптического торможения . Поэтому универсального, одинаково эффективного при всех вариантах спастического синдрома, метода лечения не существует. Однако поскольку в основе непосредственного повышения мышечного тонуса лежит патологическое усиление полисинаптических рефлексов и возбуждение спинальных мотонейронов, важным направлением медикаментозной терапии является воздействие на эти структуры .
При спастичности используются следующие методы лечения: физиотерапия и лечебная гимнастика, пероральный прием миорелаксантов, инъекции препаратов ботулинического токсина, интратекальное введение баклофена с помощью помпы, хемоденервация (фенол, алкоголизация), а также операции на сухожилиях, суставах и ризотомия. Первые три из них в настоящее время получили наиболее широкое распространение.
Физиотерапевтические методы и лечебная гимнастика наиболее эффективны в раннюю фазу возникновения спастичности и направлены на активацию естественных процессов восстановления. Ранее считалось, что одной из целей реабилитации больных, перенесших инсульт, является использование методик, в которых основной акцент делался на использовании непораженных конечностей с целью большей независимости пациентов в повседневной жизни. При этом на пораженные конечности сколько–нибудь значительная нагрузка не оказывалась. В настоящее время доказано, что активизация пораженных конечностей непосредственно влияет на процессы функциональной церебральной реорганизации и таким образом способствует лучшему восстановлению неврологического дефекта. Кроме того, чрезмерное использование больными с гемиплегией непораженных конечностей может привести к такому нежелательному явлению, как повышение тонуса в гемипаретичных конечностях . Широко используется лечение положением, тепловые и холодовые процедуры, фонофорез, чрескожная электростимуляция нервов и др. С помощью этих методик удается не только снизить повышенный мышечный тонус, но и увеличить объем движений в суставах, а также предотвратить возникновение контрактур. Все это в конечном итоге приводит к повышению функциональной активности больных. К сожалению, положительный эффект этих методов терапии, как правило, носит непродолжительный характер. К тому же до настоящего времени сколь–либо доказательные контролируемые исследования по изучению эффективности этих методик отсутствуют.
Использование препаратов ботулинического токсина более оправдано в ситуациях, когда мышечный спазм носит преимущественно локальный характер. Длительность эффекта определяется дозой введенного препарата, размером мышцы, активностью мышцы и еще рядом факторов, в том числе одновременным проведением физиотерапевтических процедур. Эффект от введения препарата сохраняется в среднем 2–6 мес. У некоторых больных может отмечаться исчезновение положительного эффекта после повторных инъекций ботулотоксина . Наиболее частыми причинами этого является неправильный выбор мышцы, в которую вводится препарат, или неадекватные дозы ботулотоксина. Однако у некоторых больных (менее 10%) может быть истинное отсутствие эффекта. Считается, что в основе этого может лежать блокирование антителами ботулотоксина типа А, однако результаты иммунологических методов исследования противоречивы . Следует заметить, что использование препаратов ботулинического токсина в значительной мере ограничено из–за их высокой стоимости.
В практической деятельности наиболее широко используются миорелаксанты – баклофен, тизанидин (Сирдалуд), диазепам, дантролен, толперизон . Среди препаратов этой группы Сирдалуд занимает особое место, что связано с механизмом его действия и клиническим эффектом. Являясь центральным a2–адренергическим агонистом, Сирдалуд обладает стимулирующим действием на моноаминергические ядра ствола головного мозга. Это приводит к торможению спинальных мотонейронов, связанных афферентными волокнами II типа со стволовыми центрами, и соответственно – к снижению мышечного тонуса. При этом уменьшается выброс возбуждающих аминокислот из вставочных спинальных нейронов. Нисходящие адренергические супраспинальные пути играют значительную роль в регуляции мышечного тонуса . Анатомически эти пути тесно связаны со спинальными структурами, особенно с передними рогами, результаты физиологических исследований свидетельствуют об их участии в регулировании рефлекторных спинальных ответов . В спинном мозге большая часть a2–рецепторов располагается на вставочных нейронах, а не на мотонейронах. Являясь производным клонидина, Сирдалуд обладает высоким сродством к a2– и практически не действует на a1–адренергические рецепторы . Под действием Сирдалуда происходит торможение высвобождения из спинальных нейронов аспартата . Этот препарат селективно ингибирует через a2–адренорецепторы вставочные нейроны задних рогов спинного мозга, что лежит в основе его анальгезирующего эффекта .
Высказывается предположение о том, что дополнительный антиспастический эффект Сирдалуда обусловлен его влиянием на a2–рецепторы норадренергических нейронов, располагающихся в области голубого пятна и оказывающих влияние на спинальные структуры . Было выявлено, что действие Сирдалуда, также как и норадреналина, на адренорецепторы не меняется на фоне введения a1– и b–адренергических антагонистов или антагониста опиатных рецепторов налоксона. В эксперименте не было выявлено действия Сирдалуда на клетки Рэншоу . D. Coward , анализируя результаты экспериментальных и клинических исследований, подчеркивает, что антиноцицептивный эффект Сирдалуда носит самостоятельный характер и не связан с его миорелаксирующим действием.
На фоне действия Сирдалуда снижается лишь тонический компонент мышечного сокращения при сохранности фазической реакции . Это отлично от действия баклофена, снижающего тонический и фазический компоненты, что сопровождается снижением силы мышц.
Таким образом, антиспастический эффект Сирдалуда связывают с несколькими механизмами действия (пресинаптическое и постсинаптическое ингибирование вставочных нейронов, возможное влияние на глутаматергическую систему). Существенным моментом является то, что Сирдалуд не противопоказан при наличии у пациентов эпилептических припадков, что делает возможным его назначение больным с постинсультными спастическими парезами и судорожными припадками. Экспериментальные данные свидетельствуют о возможном противоэпилептическом эффекте высоких доз препарата, механизм которого остается неясным . Однако в качестве собственно противоэпилептического препарата Сирдалуд не используется.
Антиспастический эффект Сирдалуда примерно сопоставим с эффектом баклофена и диазепама. Однако Сирдалуд имеет по сравнению с этими препаратами немаловажные преимущества – лучшую переносимость и отсутствие существенного снижения мышечной силы . Последнее обстоятельство существенно ограничивает использование баклофена и диазепама, поскольку снижение мышечной силы может отмечаться как в паретичных, так и в интактных конечностях. Следует заметить, что более 10% больных, начавших принимать баклофен, вынуждены в последующем отказаться от его приема из–за нарастания мышечной слабости.
Сирдалуд широко используется для лечения спастичности различного генеза . Положительный антиспастический эффект препарата носит дозозависимый характер, что подтверждается параллельным определением уровня препарата в плазме крови . Подбор индивидуально эффективной дозы (от 2 мг до максимальной дозы 36 мг/сут.) обычно осуществляется в течение 2–4 недель. После перорального приема действие препарата проявляется уже через 30–45 минут, максимальный эффект наступает в течение 1–2 часов . Улучшение отмечается у 60–82% больных (для сравнения: на фоне приема баклофена – у 60–65%, диазепама – у 60–83%), при этом спастичность снижается в среднем на 21–37% (на фоне приема плацебо – на 4–9%) .
Важно заметить, что механизм действия Сирдалуда существенно отличен от механизмов действия других препаратов, используемых для снижения повышенного мышечного тонуса. Поэтому Сирдалуд применяется в ситуациях, когда отсутствует антиспастический эффект других антиспастических средств (при так называемых «не отвечающих на лечение» случаях). Кроме того, учитывая различия в механизмах действия, Сирдалуд и баклофен могут использоваться для лечения спастичности в комбинации.
Для Сирдалуда характерен гастропротективный эффект, происхождение которого остается до конца не выясненным. Данные экспериментальных и клинических исследований свидетельствуют о его способности предохранять слизистую желудка от действия нестероидных противовоспалительных препаратов. Механизм этого эффекта связывают с адренергической активностью, торможением выработки желудочного секрета и способностью предотвращать изменения гликопротеинов, обусловленные влиянием аспирина или индометацина.
Частота возникновения таких побочных реакций, как головокружение, сонливость, сухость во рту, общая слабость, коррелирует с уровнем препарата в плазме крови . На фоне назначения Сирдалуда может отмечаться легкое снижение артериального давления , что объясняется структурным сходством этого препарата с клонидином . На здоровых добровольцах было показано, что на фоне разового приема 6–12 мг Сирдалуда снижение артериального давления составляет в среднем 10–15% . В литературе упоминается возможность Сирдалуда потенцировать действие гипотензивных препаратов .
В единичных случаях возможно преходящее увеличение уровня печеночных ферментов, исчезающее после уменьшения дозы или отмены препарата, поэтому следует осторожно назначать Сирдалуд пациентам с печеночной или почечной недостаточностью. Препарат, как правило, хорошо переносится и при длительных курсах терапии.
Литература
1. Ворлоу Ч.П., Денис М.С., Ван Гейн Ж. и др. Инсульт. Практическое руководство для ведения больных. –СПб.: Политехника, 1998. –629 с.
2. Гехт А.Б., Бурд Г.С., Селихова М.В. и соавт. Нарушения мышечного тонуса и их лечение сирдалудом у больных в раннем восстановительном периоде ишемического инсульта. //Журн. невролог. и психиатр. –1998. –Т.98, №10. –С.22–29
3. Гусев Е.И., Гехт А.Б. Спастичность. //Русск. мед. журн. –1999. –Т.7, №12. –С.567–571
4. Дамулин И.В. Постинсультные двигательные расстройства. //Consilium Medicum. –2003. –Т.5, №2. –С.64–70
5. Дамулин И.В. Принципы реабилитации пациентов, перенесших инсульт. //Справочник практического врача. –2003. –№2. –С.21–24
6. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге. /В кн.: Болезни нервной системы. Руководство для врачей. Под ред. Н.Н.Яхно, Д.Р.Штульмана. Т.1. –М.: Медицина, 2001. –С.231–302
7. Кадыков А.С. Миорелаксанты при реабилитации больных с постинсультными двигательными нарушениями. //Журн. невролог. и психиатр. –1997. –Т.97, №9. –С.53–55
8. Окнин В.Ю. Баклофен в неврологической практике. //Лечение нервных болезней. –2002. –№3. –С.34–36
9. Парфенов В.А. Лечение больных, перенесших инсульт. //Русск. мед. журн. –2001. –Т.9, №7–8. –С.306–309
10. Салихов И.Г., Богданов Э.И., Заббарова А.Т., Васильева А.В. Принципы диагностики церебральных васкулитов. –Казань: КГМУ, 2001. –27 с.
11. Behari M. Spastisity. //Neurology India. –2002. –Vol.50. –P.235–237
12. Benecke R. Spasticity/Spasms: Clinical aspects and treatment. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.169–177
13. Benecke R. Botulinum toxin for spasms and spasticity in the lower extremities. //In: Therapy with Botulinum Toxin. Ed. by J.Jankovic, M.Hallet. –New York: Marcel Dekker, 1994. –P.557–565
14. Brin M.F. Botulinum toxin: chemistry, pharmacology, toxicity, and immunology. //Muscle & Nerve. –1997. –Vol.20, suppl.6. –P.S146–S168
15. Chen D.–F., Bianchetti M., Weisendanger M. Involvement of noradrenergic systems in the modulation of cutaneous reflexes. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.179–186
16. Coward D.M. Tizanidine: Neuropharmacology and mechanism of action. //Neurology. –1994. –Vol.44., N.11 (Suppl.9). –P.S6–S11
17. Davies J. Selective depression of synaptic transmission of spinal neurons in the cat by a new centrally acting muscle relaxant, 5–chloro–4–(2–imidazolin– 2–yl–amino)– 1,3–benzothiodazole (DS103–282). //Brit. J. Pharmacol. –1982. –Vol.76. –P.473–481
18. Davies J., Johnston S.E. Inhibition by DS 103–282 of D–(3–H)–aspartate release from spinal cord slices. //Brit. J. Pharmacol. –1983. –Vol.78. –P.28–30
19. Davies J., Johnston S.E. Selective antinociceptive effects of tizanidine (DS 103–282), a centrally acting muscle relaxant, on dorsal horn neurons in the feline spinal cord. //Brit. J. Pharmacol. –1984. –Vol.82. –P.409–421
20. Davies J., Quinlan J.E. Selective inhibition of responses of feline dorsal horn neurons to noxious cutaneous stimuli by tizanidine (DS103–282) and noradrenalin: Involvement of alfa2–adrenoceptors. //Neurosci. –1985. –Vol.16. –P.673–676
21. Delwaide P.J., Olivier E. Pathophysiological aspects of spasticity in man. //In: Motor disturbances I. Ed. by R.Benecke et al. –London etc.: Academic Press, 1987. –P.153–167
22. Delwaide P.J., Pennisi G. Tizanidine and electrophysiologic analysis of spinal control mechanisms in humans with spasticity. //Neurology. –1994. –Vol.44., N.11 (Suppl.9). –P.S21–S28
23. Dietz V. Spastic movement disorder: what is the impact of research on clinical practice? //J. Neurol. Neurosurg. Psychiatry. –2003. –Vol.74. –P.820–821
24. Diez–Tejedor E., Frank A., Gutierrez M., Barreiro P. Encephalopathy and biopsy–proven cerebrovascular inflammatory changes in a cocaine abuser. //Eur. J. Neurol. –1998. –Vol.5. –P.103–107
25. Donaghy M. Toxic and environmental disorders of the nervous system. /In: Brain’s Diseases of the Nervous System. Tenth edition. Ed. by J.Walton. –Oxford etc.: Oxford University Press, 1993. –P.513–529
26. Enevoldson T.P. Recreational drugs and their neurological consequences. //J. Neurol. Neurosurg. Psychiatry. –2004. –Vol.75 (Suppl.3). –P.iii9–iii15
27. Filley C.M., Kleinschmidt–DeMasters B.K. Toxic leukoencephalopathy. //New Engl. J. Med. –2001. –Vol.345, N.6. –P. 425–432
28. Gormley M.E., O’Brien C.F., Yablon S.A. A clinical overview of treatment decisions in the management of spasticity. //Muscle & Nerve. –1997. –Vol.20, Suppl.6. –P.S14–S20
29. Gracies J.M., Nance P., Elovic E. et al. Traditional pharmacological treatments for spasticity. Part II: General and regional treatments. //Muscle & Nerve. –1997. –Vol.6 (Suppl.). –P.S92–S120
30. Groves L., Shellenberger M.K., Davis C.S. Tizanidine treatment of spasticity: a meta–analysis of controlled, double–blind, comparative studies with baclofen and diazepam. //Adv. Ther. –1998. –Vol.15, N.4. –P.241–251
31. Hassan N., McLellan D.L. Double–blind comparison of single doses of DS103–282, baclofen and placebo for suppression of spasticity. //J. Neurol. Neurosurg. Psychiatry. –1980. –Vol.43, N.12. –P.1132–1136
32. Jentsch J.D., Taylor J.R. Impulsivity resulting from frontostriatal dysfunction in drug abuse: implications for the control of behavior by reward–related stimuli. //Psychopharmacol. –1999. –Vol.146. –P.373–390
33. Joseph F.G., Scolding N.J. Cerebral vasculitis: a practical approach. //Pract. Neurol. –2002. –Vol.2. –P.80–93
34. Mayer N.H. Spasticity and the stretch reflex. //Muscle & Nerve. –1997. –Vol.20, Suppl.6. –P.S1–S13
35. Miettinen T.J., Kanto J.H., Salonen M.A., Scheinin M. The sedative and sympatholytic effects of oral tizanidine in healthy volunteers. //Anesth. Analg. –1996. –Vol.82, N.4. –P.817–820
36. Moore P.M., Richardson B. Neurology of the vasculitides and connective tissue diseases. //J. Neurol. Neurosurg. Psychiatry. –1998. –Vol.65. –P.10–22
37. Nance P.W., Sheremata W.A., Lynch S.G. et al. Relationship of the antispasticity effect of tizanidine to plasma concentration in patients with multiple sclerosis. //Arch. Neurol. –1997. –Vol.54, N.6. –P.731–736
38. Siva A. Vasculitis of the nervous system. //J. Neurol. –2001. –Vol.248. –P.451–468
39. Stein R., Nordal H.J., Oftedal S.I., Slettebo M. The treatment of spasticity in multiple sclerosis: a double–blind clinical trial of a new anti–spastic drug tizanidine compared with baclofen. //Acta Neurol. Scand. –1987. –Vol.75, N.3. –P.190–194
40. Verdejo–Garcia A., Lopez–Torrecillas F., Gimenez C.O., Perez–Garcia M. Clinical implications and methodological challenges in the study of the neuropsychological correlates of cannabis, stimulant, and opioid abuse. //Neuropsychol. Rev. –2004. –Vol.14, N.1. –P.1–41
41. Wagstaff A. J., Bryson H.M. Tizanidine. A review of its pharmacology, clinical efficacy and tolerability in the management of spasticity associated with cerebral and spinal disorders. //Drugs. –1997. –Vol.53, N.3. –P.435–452
42. Wiesendanger M. Neurobiology of spasticity. //In: Spasticity: The current status of research and treatment. Ed. by M.Emre, R.Benecke. –Carnforth etc.: The Parthenon Publishing Group, 1989. –P.45–61
43. Wiesendanger M., Palmeri A., Corboz M. Some pathophysiological considerations about muscle tone and spasticity. //In: The origin and treatment of spasticity. Ed. by R.Benecke et al. –Carnforth etc.: The Parthenon Publishing Group, 1990. –P.15–27
44. Winkler P.A. Assessment tools in the management of spasticity: Perspective from physical therapy. /In: Physiology and Management of Spasticity. Ed. C.O’Brien. –Deerfield: Discovery International, 1996. –P.3–14
45. Yatsu F.M., Grotta J.C., Pettigrew L.C. Stroke: 100 Maxims. –St. Louis etc.: Mosby, 1995
46. Young R.R. Spasticity: a review. //Neurology. –1994. –Vol.44 (Supp.9). –P.S12–S20
Инсульты представляют собой одну из важнейших современных проблем медицины. Именно инсульты являются основной причиной длительной инвалидизации. По статистике, 85% людей, перенесших инсульт, нуждаются в интенсивном курсе восстановления функциональных изменений. Проще говоря, треть больных, не получивших должного медицинского обслуживания после инсульта, становится инвалидами. Чтобы этого избежать, необходимо незамедлительно обратиться за медицинской помощью и пройти курс лечения и реабилитации.
Первые три месяца после возникновения инсульта мышечный тонус нарастает в паретичных (парализованных) конечностях, появляется легкая спастичность мышц.
На данном этапе она не является патологией. Однако нарастание мышечного тонуса приводит к ярко выраженным приступам спазмов в мышцах и развитию их контрактур. Для полного восстановления больного необходимо снять спастичность мышц, иначе он не только потеряет трудоспособность, но и не сможет самостоятельно обслуживать себя в быту.
Лечение спастики после инсульта
Восстановление после инсульта невозможно без прекращения спастичности мышц. На первом этапе реабилитации применяется ряд упражнений для ее снижения: больного укладывают в различные позы, благодаря которым спазмы проходят. Эти упражнения могут проводиться только квалифицированным медицинским персоналом и в связке с физиолечением, к которому относятся парафиновое теплолечение, нанесение аппликаций и тому подобные манипуляции. Большое значение в работе по снижению спастичности мышц имеют мануальная терапия, гимнастика и медицинский массаж.
В некоторых случаях назначается хирургическое лечение спастичности мышц, при реабилитации после инсульта этот метод лечения практически не используется.
Спустя три месяца после инсульта спастичность мышц недопустима. Именно в это время важнейшую роль в восстановлении нормального функционирования конечностей приобретают миорелаксанты. С их помощью можно снизить тонус поперечнополосатой мускулатуры, уменьшив двигательную активность мышц, вплоть до полного нивелирования их сокращений. Миорелаксанты вводятся инъекционно в области проблемных конечностей. Определяет необходимость лечения препаратами только наблюдающий врач невропатолог и только по прошествии трех месяцев с момента возникновения инсульта.
Лечение Диспортом
Одним из эффективных миорелаксантов, использующихся в нашей стране, является Диспорт. Диспорт представляет собой ботулинический токсин типа А, применяющийся для снятия спастичности мышц у больных, которые после перенесенного инсульта страдают повышенным тонусом мышц без контрактуры. У таких больных, как правило, наблюдаются мышечные спазмы, сопровождающиеся болью, а также нарушение двигательной функции конечностей.
Препарат Диспорт вводится внутримышечно в несколько инъекций.

Клинический эффект наступает только спустя некоторое время: от нескольких дней до 2 недель. Улучшение сохраняется до полугода. При этом большую важность имеет время введения инъекций. Лечение диспортом спустя год после инсульта не приведет к такому же эффекту, как лечение на ранних сроках. В этом случае легкий парез может сохраняться. Практические исследования диспорта доказали его высокую эффективность в лечении спастичности мышц руки после инсульта.
Компоненты Диспорта могут вызывать аллергию. К побочным эффектам относятся так же боли в месте инъекции и незначительные кожные высыпания. При введении диспорта в первый раз может наблюдаться общая слабость, при повторном курсе лечения, как правило, эти эффекты не наблюдаются.
Инъекции Диспорта в центре "Три сестры"
Назначать и проводить лечение Диспортом могут только квалифицированные врачи, имеющие опыт диагностики и лечения препаратом, а также прошедшие соответствующее обучение. Ни в коем случае нельзя делать инъекции у неопытного врача и без предварительного обследования. Важно знать, что побочных эффектов можно избежать при введении минимально эффективной дозы препарата.
В реабилитационном центре «Три сестры» препарат Диспорт применяется при лечении больных, проходящих курс восстановления после инсульта. Перед назначением Диспорта пациенты реабилитационного центра «Три сестры» проходят полное обследование с использованием новейшего оборудования. Специалисты центра имеют большой опыт лечения данным препаратом, регулярно проходят специализированные обучающие курсы в России и за рубежом и знают все нюансы его использования.
Как записаться на лечение
(8 800) 555 29 82 Бесплатный звонок по России
(+7 499) 755 77 75 Телефон горячей линии
Меня очень часто просят рассказать о спастике после инсульта и о том, как с ней бороться. На этот вопрос до сих пор нет 100%-но универсального ответа. Сегодня я постараюсь ответить на вопросы: как возникает спастика после инсульта и как её лечить медикаментозно.
Что такое спастика после инсульта?
Спастика после инсульта (спастичность мышц) – это гипервозбуждение рефлекса растяжения, возникающего из-за синдрома верхнего мото-нейрона.
Откуда берется спастика после инсульта?
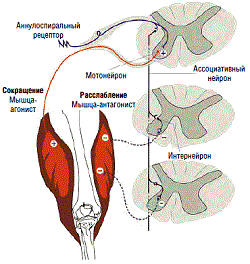
Мышцы человека, не страдающего спастикой после инсульта, во время любого действия (движение, поддержание позы) работают согласованно – одни растягиваются (агонисты), другие сокращаются (антагонисты). Причем, большая часть движений осуществляется бессознательно. Человеку не нужно думать, как изменить тонус мышц, чтобы сделать шаг. Эти процессы происходят автоматически на уровне спинного мозга. Одним из рефлексов, позволяющих бессознательно осуществлять движения — рефлекс растяжения.
Чтобы стало понятно, вспомните прием у невролога.
Врач стучит молотком по рукам и ногам, во время воздействия, руки и ноги самопроизвольно двигаются. Этот процесс обычно особенно нравится пациентам. Но что происходит? Доктор стучит по мышечному сухожилию, в момент воздействия молотка оно растягивается.
Гиперрастяжение сухожилия дает сигнал о том, что нужно запустить мышцы-антагонисты, чтобы растянутую мышцу вернуть в прежнее состояние. Это моментальная реакция, которая выражается в движении рук и ног в ответ на воздействие молотка. Данная рефлекторная дуга замыкается на уровне спинного мозга, в ней не участвует головной мозг. Но в повседневной жизни, во время движения, головной мозг всегда контролирует этот рефлекс.
Если человек не страдает спастикой после инсульта, во время движения (особенно во время резких, быстрых действий) мышцы постоянно растягиваются, но реакции, как при воздействии молотка не происходит. Головной мозг посылает специальные тормозящие импульсы, которые не дают рефлексу гипервозбуждаться. Во время сосудистой катастрофы гибнут клетки, которые посылают эти импульсы и рефлекс выходит из-под контроля. Возникает спастика после инсульта.
Механизм спастики после инсульта
Рефлекс постоянно возбуждается, любое растяжение вызывает нарастание мышечного тонуса и возникновению спастики после инсульта. Мышцы склонные к вялости – растягиваются (разгибатели руки, сгибатели ноги), мышцы склонные к напряжению – напрягаются (сгибатели руки, разгибатели ноги). Это напряжение, повышение мышечного тонуса и является спастикой после инсульта. Мышцы просто не могу расслабиться, т.к. на них постоянно воздействует рефлекс растяжения.
Как бороться со спастикой после инсульта?
На спастику после инсульта нужно обязательно воздействовать медикаментозно.
Медикаментозное лечение спастики после инсульта.
Подбор препаратов, воздействующих на спастику после инсульта, требует терпения. Нужно постепенно наращивать дозу, смотреть, как он воздействует на мышечный тонус. Если не работает – менять, опять наращивать дозу и смотреть.
Существуют 2 группы препаратов, которые могут воздействовать на спастику после инсульта:
Препараты центрального действия – обеспечивают торможение рефлекса посредствам центральной нервной системы.
- небензодиазепиновые транквилизаторы (Диазепам, Клоназепам),
- антиконвульсанты (Финлепсин, Габапентин, Прегабалин),
- альфа-адреномиметики (Клонидин).
У данных препаратов есть один минус – их прием может вызывать седативный эффект, снижение памяти, внимания, интеллекта, головокружение. Это может негативно сказываться на реабилитации. Постепенное наращивание дозы поможет снизить вероятность возникновения этих побочных эффектов.
Препараты периферического действия – “гасят” рефлекс растяжения на уровне спинного мозга. К ним относятся всем известные миорелаксанты (Мидокалм, Сирдалуд, Баклофен). Минус препаратов – общее снижение мышечного тонуса. Т.е. они снижают тонус и в спазмированных, и в растянутых мышцах. Поэтому, их прием должен обязательно сочетаться с гимнастикой.
Лечение спастики инъекциями ботулотоксина.
Следующим этапам воздействия на спастику после инсульта является применение инъекций ботулотоксина (Ботокс, Диспорт, Ксеомин). Это показано, когда тонус очень большой и другие методы не помогают. Ботулотоксин действует на уровне мышцы, блокируя импульсы рефлекса растяжения.
Очень важный момент – после инъекции ботулотоксина в течении 3-х месяцев нужно активно заниматься гимнастикой, иначе эффект будет не стойкий.